Atomimallit ja Ruthefordin koe
Tämän simulaation avulla voit tutkia Ernest Rutherfordin vuonna 1912 suorittamaa kuuluisaa koetta: https://phet.colorado.edu/sims/html/rutherford-scattering/latest/rutherford-scattering_fi.html
Simulaatiota pääset käyttämään suoraan tästä:
Koe on tunnettu siitä, että sen avulla Rutherford osoitti atomin massan keskittyneen ytimeen. Rutherford on kuvannut koettaan omin sanoin näin ”Se oli mitä ihmeellisin asia mitä minulle on koskaan elämässäni tapahtunut. Se oli yhtä uskomatonta kuin olisit ampunut tykinkuulan nenäliinaa päin ja kuula olisi pompannut liinasta takaisin osuen sinuun.”
Ennen kuin aloitat tutkimuksen simulaatiolla, kannattaa perehtyä sen taustaan lukemalla seuraava johdanto:
Nykyään tiedetään, että atomi rakentuu ytimestä ja sitä ympäröivästä elektronipilvestä. Lisäksi tiedetään, että suurin osa atomin massata on keskittynyt protoneista ja neutroneista muodostuneeseen ytimeen. Nykyään atomin mallina käytetään tyypillisesti Niels Bohrin vuonna 1913 luomaa atomimallilla. Siinä atomin keskellä on ydin, jonka ympärille elektronit ovat sijoittuneet elektronirakenteen mukaisesti. Alla on kuva Bohrin atomimallin mukaisesta neon-atomista.
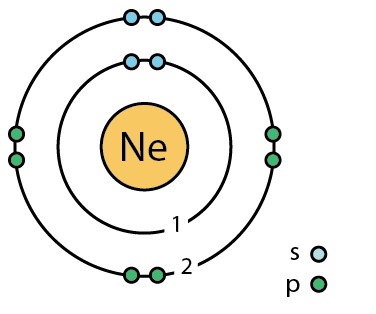
1900-luvun alussa atomin rakenna ei kuitenkaan ollut näin tarkasti tunnettu. Tuolloin kyllä tiedettiin, että
– atomit ovat kooltaan äärimmäisen pieniä (halkisijaltaan noin 10-10 metriä)
– atomi sisältää elektroneja, joiden massa on hyvin pieni osa koko atomin massata.
– atomi on sähköisesti neutraali.
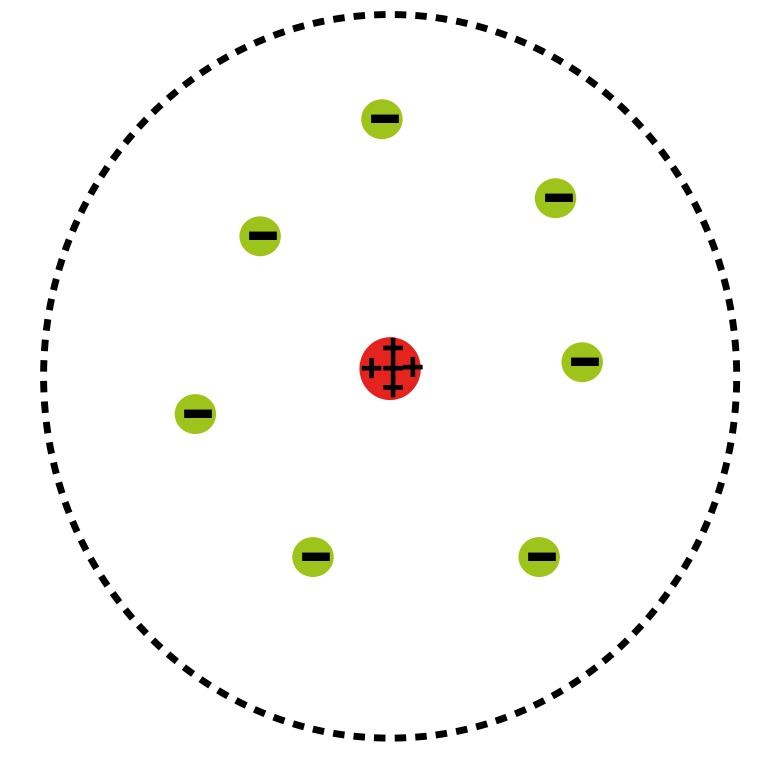
1900-luvun alussa ei kuitenkaan tiedetty, että atomilla on ydin. Atomin rakenteesta ei ollut varmuutta ja täten sen kuvaamiseksi esitetiin erilaisia malleja. Suosituin näistä atomimalleista oli J. J. Thompsonin malli, jonka perusteella pystyttiin varsin menestyksellisesti selittämään kemiallisia reaktioita. Thompsonin malli tunnetaan niin sanottuna rusinakakkumallina. Siinä negatiiviset elektronit ovat ikään kuin tasaisesti pullan sekaan sijoittuneita rusinoita. Rusinoita (elektronit) lukuun ottamatta pullan muu aines (eli taikina) muodostuu positiivisesta massasta, joka neutraloi elektronien varauksen – rusinakakkumallin mukainen atomi on siis kokonaisvarauskeltaan neutraali. Alla olevassa kuvassa on neon-atomin rusinakakkumalli (mistä tiedetään että kyseessä on juuri neon?).

Vuonna 1912 Ernest Rutherford suoritti kuuluisan kokeen, jossa hän pommitti atomeja heliumatomien ytimillä (alfahiukkasilla). Voit perehtyä tämän simulaation
https://phet.colorado.edu/sims/html/rutherford-scattering/latest/rutherford-scattering_fi.html
avulla Rutherfordin kokeeseen.
Avaa simulaatio ja suorita sen avulla seuraava tehtävä:
Valitse aluksi simulaatio ”Rusinakukkumalli”. Tutki sen avulla miten alfahiukkaset liikkuisivat atomin läpi, jos atomin rakenne noudattaisi rusinakukkumallia. Vaihda tämän jälkeen simulaatioon ”Rutherforin malli”. Tätä simulaatiota tutkimalla voit havaita mitä Rutherford kokeessaan omaksi yllätyksekseen havaitsi. Selitä millaista alfahiukkasten liike on rusinakakkumallin mukaisen atomin läpi. Selitä myös miten alfahiukkaset liikkuvat, kun ne kulkevat Rutherfordin atomimallin mukaisen atomin (eli atomin jolla on ydin) läpi.
Lisätietoja
Vaikka Thompsonin rusinakakkumalli todettiin riittämättömäksi, on hänen nimensä jäänyt historiaan, sillä häntä yleisesti pidetään elektronin löytäjänä. Rudherfordin havainnon jälkeen atomin mallina käytettiin jonkin aikaa niin sanottua Rutherfordin mallia. Siinä atomilla on positiivinen ydin, jonka ympärillä negatiiviset elektronit sijaitsevat. Alla on eräs tällainen malli – minkä atomin? Vuonna 1913 tanskalainen Niels Bohr loi nykyaikaisen käsityksen mukaisen atomimallin, jossa elektronit sijoittuvat atomin ympärille elektronirakenteen mukaisesti.
Lähteet: Tipler & Llwellyn, Modern Physics, 3. painos, s. 161, 162 ja 170, Freeman 2000, ISBN 1-57259-164-1


